Contents
再生医療の今後の展望:技術革新と市場のパラダイムシフト
エグゼクティブ・サマリー
再生医療および細胞・遺伝子治療の分野は、2024年から2030年にかけて劇的な転換期を迎える。本文書は、提供された資料に基づき、次世代技術の成熟、臨床応用の拡大、および規制・市場環境の変容を総括したものである。
主要な論点は以下の通りである:
- バイオプリンティングの高度化: 従来の押し出し方式から、VAM(体積バイオプリンティング)やDLP(デジタル光処理)による高解像度・高速造形へ移行し、複雑な血管網を持つ組織構築が可能になりつつある。
- in vivo(生体内)アプローチの台頭: 細胞を体外で加工するex vivo手法から、LNP(脂質ナノ粒子)やウイルスベクターを用いて体内で直接治療を行うin vivo CAR-Tや遺伝子編集への移行が加速している。
- AIとデジタルトランスフォーメーション: AlphaFold3などの構造解析AIや、生成AI(scGPT等)による細胞運命の予測、さらにはAI駆動型の自動製造プラットフォーム(Cellino等)が開発の効率化を牽引している。
- 新領域の倫理と規制: エクソソーム製品に対するFDAの監視強化、異種移植(ブタ臓器)の臨床入り、およびSCBEM(幹細胞由来胚モデル)に関する国際指針の策定など、技術の進歩に伴う新たな統治枠組みが求められている。
- 高額薬価と市場の成長: 遺伝子治療の薬価は最大425万ドルに達しており、アクセスの確保が課題となる一方、市場全体は年平均成長率(CAGR)最大31.27%という極めて高い成長が予測されている。
——————————————————————————–
1. バイオプリンティングと組織工学の進化
バイオプリンティング技術は、単なる細胞の積層から、機能的な臓器構築を目指す段階へと進化している。
技術方式の解像度と特性
- 押し出し方式 (Extrusion): 解像度100〜500μm、細胞密度10^7 cells/mL以上。現在も主流だが、精密な構造再現には限界がある。
- DLP方式: 解像度5〜100μm。高い造形精度を持ち、微細な構造体の構築に適している。
- VAM (体積バイオプリンティング): 断層撮影を活用し、50μm程度の解像度で数秒〜数分での高速造形が可能。細胞へのダメージを最小限に抑えることができる。
血管化 (Vascularization) 技術
組織の巨大化に不可欠な血管網の構築において、ハバード大学Wyss研究所のSWIFT (Sacrificial Writing Into Functional Tissue) 技術が注目されている。
- 高密度な細胞組織内に「犠牲材料」を用いて血管経路を書き込み、灌流可能な流路を形成する。
- 2024〜2025年には、より高度な血管網構築技術「RAPID-Vasc」への発展が見込まれている。
——————————————————————————–
2. 細胞外小胞(EV)とエクソソーム治療の現状
細胞を用いない「セルレス治療」として、EV(エクソソーム等)の臨床応用が急速に進展している。
臨床試験と標準化
- 臨床試験数: 2011年から2024年までに240件以上のEV関連の臨床試験が登録されている。そのうちMSC(間葉系幹細胞)由来のEVが大きな割合を占める。
- 国際指針 (MISEV2023): 国際細胞外小胞学会(ISEV)により、EVの定義や実験手法の標準化が進められ、in vivoでの機能評価が重視されている。
規制当局(FDA)の動向
- FDAは承認されていないエクソソーム製品に対し、2019年以降「公衆衛生上の通知」を出し、監視を強めている。
- 2026年4月までに、EV製剤の具体的な承認枠組み(PHS Act 351条に基づく生物学的製剤としての規制)がより明確化される見通しである。
——————————————————————————–
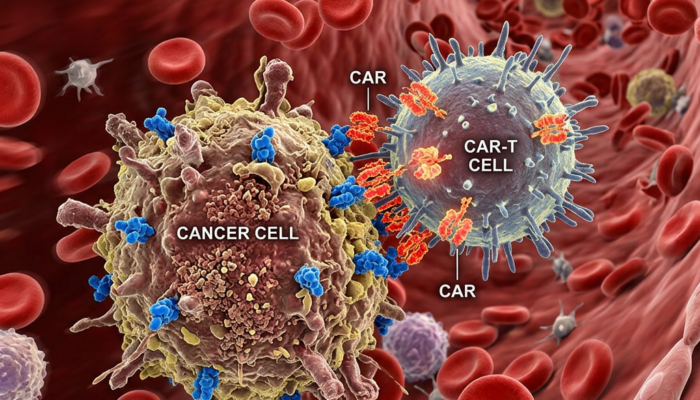
3. 次世代CAR-Tとin vivo遺伝子編集
患者から細胞を取り出す手間を省く、生体内での直接的な治療(in vivo)が新たなフロンティアとなっている。
in vivo CAR-Tの臨床入り
- Interius BioTherapeutics: 2024年10月に世界初のin vivo CAR導入治療(INT2104)の治験を開始。
- Umoja Biopharma: LNPを用いたin vivo CAR-T(UB-VV111)がFDAのファストトラック指定を受けている。
- 利点: 製造期間(通常17〜30日)の短縮、製造コスト(30万〜50万ドル)の大幅な削減が期待される。
精密遺伝子編集 (Base/Prime Editing)
- 塩基編集 (Base Editing): DNAを切断せずに1塩基を置換する。Beam Therapeuticsが鎌状赤血球症を対象とした治験(BEAM-101)を推進中。
- プライム編集 (Prime Editing): より複雑な挿入・置換を可能にする技術。Prime MedicineがCGD(慢性肉芽腫症)を対象とした治験を2024年に開始した。
——————————————————————————–
4. AIと自動化による開発・製造の変革
デジタル技術の統合が、再生医療のR&Dおよび供給体制を根底から変えつつある。
構造解析AIと基盤モデル
- AlphaFold3: Google DeepMindが開発。タンパク質だけでなく、DNA、RNA、低分子化合物との相互作用を高精度に予測し、創薬を加速させる。
- scGPT / CellFM: 数千万個のシングルセルデータを学習したAI基盤モデル。未知の細胞状態や治療反応の予測に活用される。
AI駆動型自動製造
- Cellino Biotech: AIとレーザー技術を組み合わせたiPSC由来細胞の自動製造プラットフォーム「Nebula」を開発。2025年にはFDAの「高度製造技術(AMT)」指定を受ける可能性がある。
- 自動化のインパクト: 熟練者の技能に依存しない安定供給と、大規模なコスト削減を実現する。
——————————————————————————–
5. 異種移植と倫理的・社会的論点
深刻なドナー不足を解消する手段として、動物臓器の活用や人工的な胚モデルの研究が進んでいる。
異種移植 (Xenotransplantation)
- eGenesis: 69箇所の遺伝子改変を施したブタの臓器を用いて、ヒトへの移植試験を開始。
- 臨床実績: 遺伝子改変ブタ腎臓の移植を受けた患者が生存し、機能した事例が報告されている(2024年、MGH等)。
- 課題: 内因性レトロウイルス(PERV)の感染リスクや、免疫拒絶の完全な制御が焦点となる。
幹細胞由来胚モデル (SCBEM)
- iPS/ES細胞からヒト胚に類似した構造を構築する研究が進展。
- ISSCR 2025 ガイドライン: 胚モデルのカテゴリー分類(統合型・非統合型)や、培養期間の制限、生殖目的の使用禁止など、倫理的枠組みが更新される。
——————————————————————————–
6. 市場展望と経済的課題
再生医療市場は爆発的な成長が見込まれる一方、極めて高い薬価が持続可能性の議論を呼んでいる。
市場予測と成長率
- 市場規模: 2034年にかけてのCAGR(年平均成長率)は、調査機関により8.4%から31.27%と予測されている。
- 成長要因: 承認済製品の適応拡大、他家(アロ)細胞製剤の上市、および製造技術の効率化。
薬価の現状(主要製品例)
| 製品名 | 対象疾患 | 薬価 (米ドル) |
| Lenmeldy | 異染性白質ジストロフィー | 425万ドル |
| Hemgenix | 血友病B | 350万ドル |
| Elevidys | デュシェンヌ型筋ジストロフィー | 320万ドル |
| Casgevy | 鎌状赤血球症 | 220万ドル |
これらの超高額治療薬に対し、支払能力や医療保険制度の維持が国際的な課題となっている。
——————————————————————————–
本資料は提供されたソースコンテキストに基づき作成されました。








コメント