Contents
整形外科・スポーツ医学における再生医療:最新動向と臨床的エビデンスに関する要約報告書
エグゼクティブ・サマリー
本報告書は、整形外科およびスポーツ医学の分野における再生医療の現状、主要な技術、臨床的エビデンス、および規制の枠組みを包括的にまとめたものである。現在、この分野は従来の外科的手法から、細胞治療、血小板由来因子、組織工学を組み合わせた「オーソバイオロジクス(Orthobiologics)」へと大きくシフトしている。
主要なポイントは以下の通りである:
- 疾患動向: 変形性膝関節症(KOA)の潜在患者数は2,530万人に達し、高齢化社会において再生医療の需要が極めて高い。
- 主要技術: 間葉系幹細胞(MSC)、多血小板血漿(PRP)、骨髄吸入濃縮液(BMAC)に加え、BEAR®やMACI®といった革新的な組織工学製品が市場を牽引している。
- 規制と課題: 「医薬品、医療機器等の品質、有効性及び安全性の確保等に関する法律(薬機法)」に基づき、2024年から2025年にかけて新たな承認やガイドラインの更新が予定されている。また、過去のINFUSE®(BMP-2)の事例から、オフラベル使用の管理と透明性の高いエビデンス構築が課題となっている。
- 臨床的有効性: 多くのメタ解析により、PRPやMSCが従来のヒアルロン酸(HA)治療を上回る疼痛改善効果を示すことが示唆されているが、標準化(MIBO等)が今後の普及の鍵となる。
——————————————————————————–
1. 規制の枠組みと市場動向
整形外科分野における再生医療は、厳格な法的規制の下で進展している。
- 薬機法の影響: 2014年11月の施行以来、再生医療等製品の早期承認制度が導入された。2024年6月から2025年5月にかけて、既存の枠組みの更新と新たな承認プロセスが進行中である。
- 主要な承認製品:
- MACI®: 自家培養軟骨。FDAにより2016年に承認。18〜54歳の膝軟骨欠損を対象とする。
- BEAR®: 前十字靭帯(ACL)修復用スキャフォールド。2020年にFDAのDe Novo承認を取得。
- Osteopore®: 3Dプリント技術を用いたPCL-TCP製の骨欠損補填材。
——————————————————————————–
2. 再生医療の主要なモダリティと技術
整形外科で用いられる主な治療手段は、以下の3つのカテゴリーに分類される。
2.1 細胞治療 (Cells)
- MSC(間葉系幹細胞): 骨髄由来(BM-MSC)、脂肪由来(AD-MSC)、臍帯由来(UC-MSC)などが用いられる。
- iPS細胞: 日本を中心に、iPS細胞由来軟骨(hiPS-Cart)の臨床研究が2024年7月時点で進行中である。
2.2 血液・骨髄由来因子 (Blood/Bone Marrow Derived)
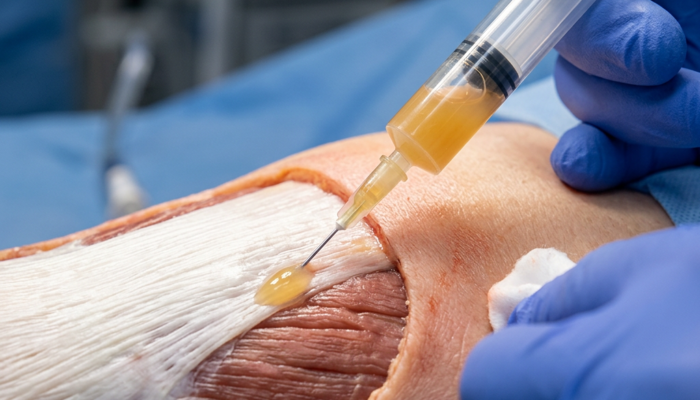
- PRP(多血小板血漿): 成長因子を放出し、組織修復を促進する。Marxの提唱によれば、1,000,000個/µL以上の血小板濃度が目安とされる。
- BMAC(骨髄吸入濃縮液): 幹細胞と成長因子の両方を含み、骨壊死(ONFH)や偽関節の治療に有効。
2.3 組織工学とスキャフォールド (Scaffolds)
- 3Dプリンティング: 患者個別の解剖学的形状に合わせた補填材の作成。
- コラーゲン製スキャフォールド: BEAR®のように、自己血を保持して組織再生の足場となる技術。
——————————————————————————–
3. 臨床応用:部位別の詳細分析
3.1 膝関節疾患
膝関節は再生医療の最大の市場である。
- 変形性膝関節症 (KOA):
- ROADスタディによれば、40歳以上の有病率は男性42.6%、女性62.4%に達する。
- Kellgren-Lawrence(KL)分類グレード2〜3の症例が、PRPやMSCの主要な適応対象となる。
- 前十字靭帯 (ACL):
- 従来の再建術(BPTB法等)に対し、自己靭帯の治癒を促進するBEAR®治療が登場。
- BEAR II試験(n=100)では、IKDCスコアおよび前方不安定性の改善において、再建術と同等の成果が報告されている。
- 半月板:
- 血管の乏しい「ホワイトゾーン」の損傷に対し、CMI(Stryker社)やActifitなどのスキャフォールドを用いた修復が試みられている。
3.2 股関節および肩関節
- 大腿骨頭壊死 (ONFH): HernigouらによるBMAC治療の長期成績では、Stage I/IIの早期症例において、10年後の人工股関節置換術(THA)への移行を大幅に遅らせる効果(87%が回避)が確認されている。
- 腱板断裂: PRP(特にLP-PRP)の併用が、再断裂率の低下と術後疼痛の改善に寄与するというメタ解析結果(Hurley, 2021)がある。
3.3 脊椎疾患と骨欠損
- 椎間板性腰痛: Mesoblast社のMSC製品(rexlemestrocel-L)のフェーズIII試験(n=404)において、有意な疼痛改善効果(p=0.008)が示された。
- 骨癒合促進: INFUSE®(rhBMP-2)は、2002年のFDA承認以来、腰椎前方固定術(ALIF)に革命をもたらしたが、副作用とオフラベル使用が問題となった。
——————————————————————————–
4. 臨床的エビデンスの集約(メタ解析結果)
ソース内で引用されている主要なエビデンスは以下の通りである。
| 対象疾患 | 比較内容 | エビデンスの結論 | 出典 |
| KOA | PRP vs ヒアルロン酸 | 18件のRCT解析で、PRPが有意に優る疼痛改善を示す | Belk (2021) |
| 腱板断裂 | LP-PRPの併用 | 13件のRCT解析で、再断裂率を有意に低下させる | Hurley (2021) |
| ACL修復 | BEAR® vs 再建術 | 6年間の追跡で、BEAR®が再建術と同等の機能維持を確認 | Fleming (2024) |
| 椎間板 | MSC注入 | 3ヶ月時点で疼痛の有意な改善を確認 | Mesoblast PhIII |
——————————————————————————–
5. 安全性と教訓:INFUSE® (BMP-2) の事例
Medtronic社のINFUSE®は、再生医療における「光と影」を象徴する事例として詳述されている。
- 成功と普及: 2002年の承認後、骨融合率94.5%(自家骨88.7%に対し優位)という高い成績を収めた。
- 不適切な使用と訴訟:
- 全使用の約85%がオフラベル(承認外使用)であった。
- 2008年の公衆衛生通知により、頸椎への使用による深刻な合併症(気道閉塞等)が報告された。
- Medtronic社は、False Claims Act違反等により、総額数億ドルの和解金を支払うに至った(2011年:2.35億ドル、2012年:0.85億ドル等)。
- 教訓: 再生医療等製品の普及には、販売促進の透明性と、予期せぬ副作用に対する厳格な監視体制が不可欠である。
——————————————————————————–
6. 今後の展望と標準化
再生医療が標準治療として定着するためには、治療法の「標準化」が急務である。
- MIBOの推進: オーソバイオロジクスにおける最小限の情報報告基準(Minimum Information for Biologics in Orthopaedics)の確立が求められている。
- 次世代技術: エクソソーム(EV)や、より高濃度の細胞投与(Superdose)の研究が進んでおり、個別化医療の進展が期待される。
- 2026年問題: 多くの進行中のRCT(MautnerらのORBI試験等)が2026年4月までに結果を出す予定であり、この時期が整形外科再生医療の転換点となると予測される。






コメント